Un ulcère du pied diabétique, une complication grave du diabète – voici pourquoi.

Avertissement : images graphiques
Le diabète est l’une des maladies les plus courantes dans le monde. En 2015, la prévalence estimée du diabète était de 3,4 millions, soit 9,3 % de la population, et devrait atteindre 5 millions ou 12,1 % de la population d’ici 2025, ce qui représente une augmentation de 44 % de 2015 à 20251.
Les complications à long terme sont progressives, avec une plus grande possibilité de se développer chez les personnes vivant avec le diabète pendant plusieurs années. Avec de 15 % à 25 % des patients atteints de diabète à risque, les ulcères du pied diabétique sont l’une des complications les plus graves. De plus, à mesure que les ulcères du pied diabétique s’aggravent, le risque d’amputation augmente – près de 84 % des patients qui subissent une amputation des membres inférieurs présentaient un ulcère du pied diabétique avant l’amputation.
Les ulcères du pied diabétique sont généralement classés selon la profondeur de la blessure et la présence d'une infection. Plusieurs systèmes de classification pour les ulcérations du pied diabétique ont été créés, y compris le système de classification Wagner le plus largement utilisé.
Ce système classe l’ulcère du pied diabétique en fonction de divers facteurs, tels que la profondeur de pénétration. Il attribue une note basée sur la gravité – le grade 1 étant le plus bas (ulcère diabétique superficiel) et le grade 5 étant le plus élevé (gangrène du pied entier)2.
Comment l’ulcère du pied diabétique se développe : une gamme de facteurs de risque.
Il existe une variété de causes pour le développement de l’ulcération du pied diabétique. Certaines des plus communes sont la neuropathie périphérique, la maladie artérielle périphérique, une malformation du pied, le diabète mal contrôlé, et le tabagisme.
La neuropathie périphérique peut se manifester comme l’un des trois types suivants : la neuropathie sensorielle, la neuropathie motrice et la neuropathie autonome. Dans le premier type, le patient n’est pas au courant de la dégradation de la peau due à une perte sensorielle. Dans le second, les muscles intrinsèques du pied peuvent être affectés, provoquant une malformation et un déséquilibre musculaire, et pourraient conduire à un ulcère du pied diabétique. En neuropathie autonome, la peau sèche et fissurée, et la diminution de la transpiration, pourraient rendre le patient vulnérable à la dégradation de la peau et à une infection possible3.
La maladie artérielle périphérique (MAP) endommage les artères inférieures des membres. En présence de MAP dans un ulcère du pied diabétique, l’amputation des membres inférieurs devient une possibilité, en particulier lorsque des pertes tissulaires et des infections importantes se sont produites4, 5. Les signes et symptômes comprennent de la douleur lors de la marche ou du repos, une peau serrée et brillante, des ongles d’orteil épaissis et cassants, un manque de croissance des cheveux sur le pied ou la jambe.
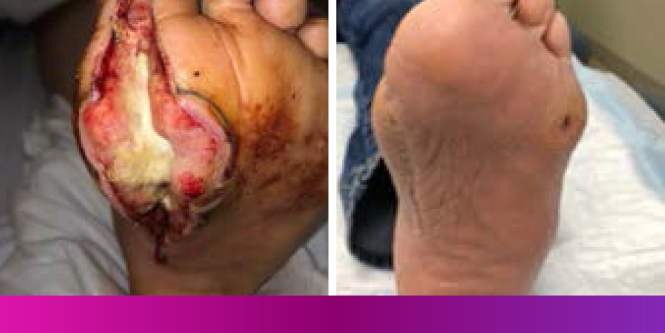
Image choquante – Cliquez pour révéler
De plus, les malformations structurales dans le pied pourraient entraîner des pressions mécaniques anormales et des lésions cutanées. Les malformations courantes incluent des malformations d’orteil en marteau, des malformations d’orteil en griffe, une tête du métatarsien proéminente, l’atrophie du coussinet adipeux plantaire, le pied creux (voûte plantaire haute), la malformation de pied de Charcot, et l’équinisme (mouvement de flexion vers le haut limité de l’articulation de cheville) sont quelques malformations communes vues dans le pied diabétique6, 7, 8.
Lorsque la glycémie est élevée, les globules blancs sont affectés. Si les globules blancs d’un patient ne fonctionnent pas correctement et que son diabète n’est pas contrôlé, le patient devient plus vulnérable à l’infection et son corps est incapable de guérir les plaies. Cela peut entraîner d’autres complications telles que la cellulite et l’ostéomyélite9, 10.
Un ulcère du pied diabétique ne devrait pas demeurer ouvert longtemps.
Il y a une possibilité de développer une ostéomyélite si l’ulcère du pied diabétique demeure ouvert, et le risque de ceci augmente, plus l’ulcère demeure non traité. L’ostéomyélite est une complication dévastatrice et peut entraîner un débridement osseux ou, pire encore, une amputation.
Les essais comme la radiographie simple, les tomodensitogrammes, la médecine nucléaire, l’imagerie par résonance magnétique (IRM), et les marqueurs inflammatoires, y compris le taux de sédimentation d’érythrocyte (ESR) et la protéine C réactive (CRP), peuvent aider à diagnostiquer l’ostéomyélite. Pour les patients atteints d’un ulcère du pied diabétique, commencez par une radiographie de base. Si les soins conventionnels de plaie échouent ou si la plaie s’étend à des structures plus profondes, y compris une sonde positive à l’os, utilisez un imageur évolué.
|
Image choquante – Cliquez pour révéler |
Image choquante – Cliquez pour révéler |
Gérer les ulcères du pied diabétique dans le monde réel.
Dans la gestion des ulcères du pied diabétique, l’objectif principal est de prévenir l’amputation en fermant la plaie le plus rapidement possible. Le débridement, le déchargement (un élément essentiel de la gestion de l’ulcère du pied diabétique), le traitement de toute infection et/ou inflammation sous-jacente, la gestion de l’exsudat des plaies et la promotion des bords des plaies devraient tous être inclus dans le traitement des plaies11, 12.
L’étalon de référence pour les patients est le plâtre de contact total. Lorsque ce n’est pas une option, les marchettes à mouvement contrôlé de la cheville devraient être envisagées, ainsi que l’utilisation de fauteuils roulants, de marchettes et de chaussures modifiées13.
Des solutions médicales qui pourraient aider à la guérison des plaies.
Le traitement des plaies par pression négative (TPN) est une autre façon d’aider à créer un environnement qui favorise le processus de guérison des plaies. L’application d’une pression négative sur une plaie aide également à éliminer des liquides de la plaie, qui peuvent inclure des matières infectieuses. La cicatrisation des plaies peut être facilitée à l’aide du traitement des plaies par pression négative (TPN), qui gère l’exsudat excessif de la plaie. Selon la taille de la plaie, certaines options de TPN comprennent le Système de thérapie ActiV.A.C.MC 3MMC ou le Système de thérapie jetable SnapMC 3MMC.
Le Système de thérapie ActiV.A.C.MC 3MMC est un système de traitement des plaies par pression négative portable conçu pour le malade sur pied. L’unité de thérapie est destinée à aider les patients à reprendre leurs activités de la vie quotidienne, tout en recevant les avantages éprouvés de guérison des plaies, grâce au Système de thérapie ActiV.A.C.MC 3MMC.
Le Système de thérapie SnapMC 3MMC est petit et discret, car il peut être caché sous les vêtements. Il aide le patient à préserver sa qualité de vie car il y a une interférence minimale avec la vie quotidienne, même lorsqu’il est dans un cadre social ou qu’il dort.
|
Image choquante – Cliquez pour révéler |
Image choquante – Cliquez pour révéler |
Il ne fait aucun doute que les blessures au pied diabétique sont une complication grave qui pourrait mener à l’amputation. Il est extrêmement important d’identifier ses causes le plus tôt possible afin de traiter efficacement les plaies, en particulier les ulcères. Des solutions médicales comme la Matrice d’équilibrage des plaies Promogran PrismaMC 3MMC, le Système de thérapie ActiV.A.C.MC 3MMC ou le Système de thérapie SnapMC 3MMC peuvent être utilisées pour aider la guérison des plaies. Pour en savoir plus sur les Solutions 3M, utilisez le graphique Solutions pour le traitement des plaies actif et évolué et l’intégrité de la peau ou communiquez avec un représentant ci-dessous.
Exonération de responsabilité : Ces renseignements ne doivent pas se substituer aux conseils, au diagnostic ou aux traitements prodigués par un professionnel de la santé. Veuillez demander conseil à un médecin si vous avez des questions au sujet de cet état de santé particulier. La lecture du présent document ne devrait pas vous inciter à ignorer l’avis de votre fournisseur de soins de santé ou à reporter une telle consultation.
Bibliographie :
1 : Diabetes Canada, Statistiques sur le diabète au Canada, 2017. Disponible à l’adresse :
2 : Oyibo S.O., Jude E.B., Tarawneh I., Nguyen H.C., Harkless L.B., Boulton A.J., « A comparison of two diabetic foot ulcer classification systems: the Wagner and the University of Texas wound classification systems », Diabetes Care, vol. 24, n° 1 (2001), pp. 84 à 88.
3 : Sumpio B.E., « Contemporary evaluation and management of the diabetic foot. », Scientifica (Cairo), vol. 2012, no d’article 435487, 2012.
4 : Won S.H., Chung C.Y., Park M.S., Lee T., Sung K.H., Lee S.Y. et coll., « Risk factors associated with amputation-free survival in patient with diabetic foot ulcers », Yonsei Med J., vol. 55, no 5 (2014), pp. 1 373 à 1 378.
5 : Akbari C.M., LoGerfo F.W., .« Microvascular changes in the diabetic foot », dans éd. Veves A., Giurini J.M., LoGerfo F.W., The Diabetic Foot, 1re édition, Totowa, NJ, Humana Press, 2002, pp. 99 à 112.
6 : Bus S.A., Maas M., Michels R.P., Levi M., « Role of intrinsic muscle atrophy in the etiology of claw toe deformity in diabetic neuropathy may not be as straightforward as widely believed », Diabetes Care, vol. 32, no 6 (2009), pp. 1 063 à 1 067.
7 : van Schie, C.H.; Vermigli C., Carrington A.L., Boulton A., « Muscle weakness and foot deformities in diabetes: relationship to neuropathy and foot ulceration in caucasian diabetic men », Diabetes Care, vol. 27, no 7 (2004), pp. 1 668 à 1 673.
8 : Heitzman, J., « Foot care for patients with diabetes », Top Geriatr Rehabil, vol. 26, no 3 (2010), pp. 250 à 263.
9 : Wild T., Rahbarnia A., Kellner M., Sobotka L., Eberlein T., « Basics in nutrition and wound healing », Nutrition, vol. 26, no 9 (2010), pp. 862 à 866.
10 : Sharp A., Clark J., .« Diabetes and its effects on wound healing », Nurs Stand, vol. 25, no 45 (2011), pp. 41 à 47.
11 : Schultz G.S., Sibbald R.G., Falanga V., et coll., « Wound bed preparation: a systematic approach to wound management », Wound Repair Regen., vol. 11, suppl. 1 (2003), pp. S1 à S28.
12 : Chadwick P., Edmonds M., McCardle J., Armstrong D., « Best Practice Guidelines: Wound management in diabetic foot ulcers. », Wounds Int., 2013, pp. 1 à 23.
13 : Snyder R.J., Hanft J.R., « Diabetic foot ulcers - effects on quality of life, costs, and mortality and the role of standard wound care and advanced-care therapies in healing: a review », Ostomy Wound Manage., vol. 55, no 11 (2009), pp. 28 à 38.



